在现代肿瘤学百余年历程的三次革命性突破中,调动患者全身天然免疫功能的免疫疗法作为第三次变革,成为肿瘤免疫治疗的爆发点。
肿瘤免疫治疗行业概况
癌症发病率逐年上升,推进肿瘤治疗市场发展
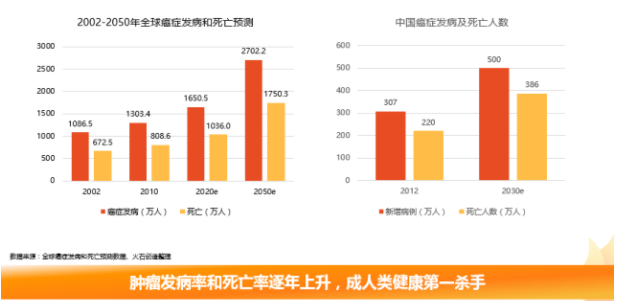
随着全球人口不断的增长与老龄化的加剧,肿瘤的发病率和死亡率逐年上升,已经成为危害人类健康的第一杀手。根据全球癌症发病和死亡预测数据显示,2010年全球癌症发病人数达到1303万人,死亡人数约808万人,预计到2050年,全球癌症发病人数将达到2702万人,约有1750万人死于癌症。
我国的情况亦是如此。据不完全统计,2012年我国新增癌症病例约307万例,其中约220万人死于癌症,预计到2030年我国新增癌症病例将达到500万人,死亡人数将达到386万人。
肿瘤发病率/死亡率的不断升高,推动抗肿瘤药物市场不断高速发展。据IMS数据显示,2014年全球用于治疗肿瘤的药物费用为1000亿美元,远高于其他疾病的用药开销,成为全球第一大药物市场。
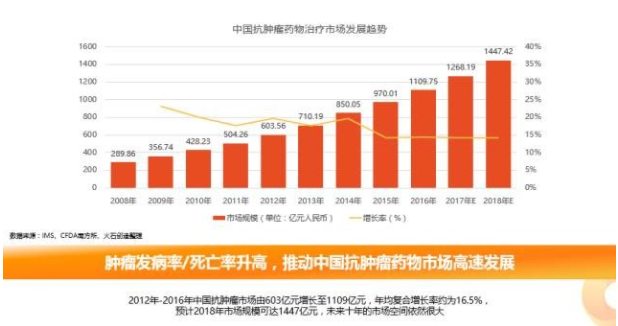
我国抗肿瘤药物市场规模也呈逐年上升趋势,从2012年的603亿元增长至2016年的1109亿元,年均复合增长率约为16.5%,预计2018年市场规模可达到1447亿元,未来十年的市场空间依然很大。
免疫治疗成为第四大肿瘤治疗技术
自人类首次认识肿瘤以来,先后开发了手术切除、化疗、放疗等治疗手段。然后随着肿瘤学与免疫学发展的不断深入,围绕人体免疫系统来治疗肿瘤逐步被接受。2013年《Science》将肿瘤免疫治疗评选为年度十大科学突破之首。
在现代肿瘤学的百余年历程中,先后实现了三次革命性的突破。第一次是细胞毒性化疗药物的发现,改变了肿瘤治疗依靠手术和放疗的局面;第二次是靶向治疗,提高了抗肿瘤药物的治疗指数,为精准医疗奠定了基础;第三次就是调动患者全身天然免疫功能的免疫疗法。
肿瘤免疫治疗发展增速
所谓肿瘤免疫治疗,是指在治疗过程中直接或间接利用人体免疫系统对肿瘤患者进行有效治疗的方法。人类对其的研究在经历了20世纪的狂热期和质疑期后,在21世纪逐渐进入复苏期,自2010年FDA批准首个治疗前列腺癌的肿瘤疫苗Provenge后,肿瘤免疫治疗发展明显加快。
治疗性肿瘤疫苗、免疫检查点抑制剂、过继细胞免疫治疗是目前主要技术分类。其中治疗性肿瘤疫苗是领域内最早的应用,全球首个治疗性肿瘤疫苗Melacine由Corixa公司原研,于1999年在加拿大上市,用于晚期黑色素瘤的治疗。而免疫检查点抑制剂是目前领域内应用最成熟的一类。
Yervoy是由百时美施贵宝研发的,于2011年在美国上市的全球首个免疫检查点抑制剂,用于治疗黑色素瘤。今年8月30日,全球首个CAR-T细胞疗法Tisagenlecleucel比预计时间提早一个月获批。
肿瘤免疫治疗市场规模有望突破千亿美元
随着重磅产品陆续获批上市,肿瘤免疫治疗已经成为全球生物医药界备受瞩目的新星。据ClinicalTrial的统计数据显示,截至2017年8月,全球共有1707例临床免疫治疗研究,其中美国1017例,中国大陆注册了172例,约占总数的10.08%。免疫治疗已经成为肿瘤治疗研究的热点领域。
基础研究突飞猛进,加之大量临床转化的加速推进,及相应的监管法规的进步与健全,为行业的发展保驾护航。据Markets and Markets的数据预测,全球肿瘤免疫治疗市场规模将从2016年的619亿美元增长到2021年的1193.9亿美元,年复合增长率达到14.0%。
我国政策趋紧,产业监管逐步规范化
2015年前,国内免疫疗法的临床应用“开着大门,却没有让进”。2015年7月,国家卫计委发布取消第三类技术准入审批,此类技术临床应用和管理的责任主体只由医疗机构承担。
“魏则西事件”后,国家卫计委医政医管局就规范医疗机构科室管理及医疗技术临床应用管理做出规定,其中一条就是要求细胞免疫治疗必须停止应用于临床治疗,仅限于临床研究。
2016年12月,CFDA发布了《细胞制品研究与评价技术指导原则》(征求意见稿),第一次明确细胞免疫治疗产品的药物属性。

肿瘤免疫治疗产业图谱
我们扫描了国内肿瘤免疫治疗领域的92家企业,按照过继细胞免疫治疗、免疫检查点抑制剂、个性化肿瘤疫苗的标签分类。
从国内研发企业累计数量分析,在经历了2015年相对快速的增长后,企业新增数量趋缓。其中布局过继细胞免疫疗法的企业数量相对其他两个细分领域较多。
从领域内企业的地域分布分析,上海是落户企业最多的地区,其中过继细胞免疫疗法的企业最多。西比曼、吉凯基因、科济生物、恒润达生、药明巨诺、复兴凯特等纷纷选择上海。
除此以外,近年来深圳市以“孔雀计划”大力引进海外高层次人才,支持包括细胞免疫疗法在内的生物医药产业发展,吸引了一批细胞免疫治疗类创新型企业落户深圳。
产业细分领域
在肿瘤免疫治疗的三种技术疗法中,治疗性肿瘤疫苗获批最早,其后几款重磅产品纷纷上市。纷争最多的过继细胞免疫疗法也在今年8月30日迎来首个产品。
免疫检查点单抗

免疫治疗未来核心所在
免疫检查点单抗疗法是通过调节T细胞活性来提高抗肿瘤免疫反应的治疗方法。目前热门靶点包括CTLA-4、PD-1、PD-L1等,与基因组靶向药物联合用药后,具有可持续的疗效,且中位存活率显著提高。
相比另两个,免疫检查点抑制剂是目前应用最成熟的领域,已经有6个产品上市,分别是CTLA-4单抗Yervoy、PD-1单抗Opdivo和Keytruda,及PD-L1单抗Tecentriq、Bavencio和Imfinzi。
目前国内超过20家企业正在申报免疫检查点单抗候选产品的临床试验,研究的靶点基本集中在PD-1/PD-L1,且申报临床的数量逐年增加。
过继细胞免疫治疗
中国已经跻身CAR-T临床研究第一梯队
过继细胞免疫治疗(ACT)是指通过对自体免疫细胞进行体外激活和扩增,然后将其重新输回肿瘤患者体内,并辅以合适的生长因子,促使其发挥杀伤杀死肿瘤细胞的功能。与免疫检查点抑制剂相比,过继细胞免疫疗法不会产生耐药性,可调动免疫体系更好靶向追踪杀灭肿瘤。
其经历了五代的发展,从最早的淋巴因子激活的杀伤细胞(LAK,第一代),到第二代细胞因子诱导的杀伤性细胞(CIK,至第三代肿瘤浸润性淋巴细胞(TIL),进而是第四代抗原特异性的细胞毒性T淋巴细胞(CTL),已经发展到第五代嵌合抗原受体T细胞(CAR-T)。
2017年8月30日,美国FDA批准诺华CAR-T疗法Tisagenlecleucel(曾用名CTL019)上市,用于复发或难治性儿童和年轻成人急性淋巴白血病(ALL),使之成为FDA批准的第一基因治疗药物。诺华为其定价47.5万美元。

当前,国内大部分企业主要布局在CIK细胞和没有抗原负载的DC-CIK领域。随着CAR-T临床研究的热度上升,以及国家政策支持,国内越来越多的企业开始布局CAR-T、TCR-T技术。
美国是全球开展CAR-T细胞疗法临床试验最早的国家,在2010年以前,全球注册的CAR-T临床试验基本集中在美国。到2012年开始,中国301医院开始注册CAR-T临床试验。据ClinicalTrial.gov的数据显示,截至今年8月,中国登记开展的CAR-T临床研究项目达110项,已经在数量上超过欧洲,仅次于美国,超过全球注册总数的40%,并呈逐年递增趋势。
从国内在ClinicalTrial上注册的临床项目分析,CD19是临床研究中最热门的靶点,占到总数的26%。开展临床最多的医疗机构主要是第三军医大学西南医院、中国人民解放军总医院301医院、上海交通大学医学院附属医院仁济医院等。
随着中国跻身CAR-T临床研究第一梯队,我们认为,在技术属性和可复制性都较强的CAR-T领域,我国存在弯道超车的可能性。
治疗性肿瘤疫苗
基于新抗原的个性化肿瘤疫苗将为研究迎来暖春
肿瘤疫苗并不是新概念,比如HBV疫苗、HPV疫苗等,但这都是预防性肿瘤疫苗。治疗性肿瘤疫苗的疗效与其近100%有效率相比有天壤之别,由于价格昂贵、生产及使用极为复杂,因此该领域在前几年处于颓势。国内布局该领域的企业也相对较少。
目前为止,FDA仅在2010年批准了一个治疗性肿瘤疫苗Provenge,由Dendreon公司原研,用于治疗晚期前列腺癌。Provenge上市第一年销售额达4.8亿美元,而后由于失败的市场推广策略等原因,销售额开始走低,Dendreon公司也因此被Valeant公司收购。

今年1月,国内的三胞集团以8.19亿美元的价格将Dendreon公司从Valeant公司手中收购,成为全球首个治疗前列腺癌肿瘤疫苗的拥有者。Provenge的命途多舛只能说是经济学上的失败,而其有效性已经说明了治疗性肿瘤疫苗在肿瘤免疫治疗中扮演了重要角色。
目前,全球有50多个治疗性肿瘤疫苗正在临床试验阶段,覆盖黑色素瘤、肺癌、乳腺癌等。今年,肿瘤疫苗的研究有了可观的进展。Nature的两篇文章报道了两项基于新抗原的个性化疫苗独立试验的积极临床结果,针对肿瘤突变定制的个性化疫苗,在黑色素瘤患者治疗中获得巨大成就。
个性化肿瘤疫苗与传统的肿瘤疫苗不同,其通过发现患者体内特异性表达的肿瘤新抗原,继而个性化激活免疫系统,将一定意义上实现个性化精准医疗。
关于肿瘤新抗原的概念,事实上,这种肿瘤细胞在快速生长和增值的过程中出现的新突变蛋白,早在2013年就通过NGS技术被发现。但此前科学家认为大多数肿瘤新抗原所携带的突变本身对肿瘤细胞的成长并没有影响,随着研究的深入,才发现即使同种患者身上的突变也不尽相同,新抗原可作为特异的标志物被免疫细胞识别。
产业投资数据
据火石创造统计,国内肿瘤免疫治疗产业公开披露融资51次(包括IPO/新三板挂牌),披露总融资金额约88.37亿元人民币,平均单笔融资约1.73亿元。单笔过亿元融资19笔,超十亿元融资达3笔。
从融资阶段分析,国内肿瘤免疫治疗的投融资主要集中在早期阶段,2016年融资数量与上一年相比有一定的减少,但单笔融资金额却较2015年增加。
从细分领域获得的融资分析,免疫检查点单抗和过继细胞免疫治疗各披露融资23笔,但披露融资金额则相差甚大,分别为63.65亿元和6.83亿元。
免疫检查点单抗是近年领域内投资热点,但从细分领域历年融资数量分析,资本对过继细胞免疫疗法的关注度逐渐提高。资本的助力将进一步推进细胞免疫治疗的临床研究进展。
从领域内披露融资金额TOP10的企业分析,不难发现,国内巨额融资基本集中在布局免疫检查点抑制剂的企业。其中药明康德不仅涉及到免疫检查点单抗的研发,亦与细胞疗法巨头之一的JUNO公司合作布局CAR-T细胞疗法的研发。
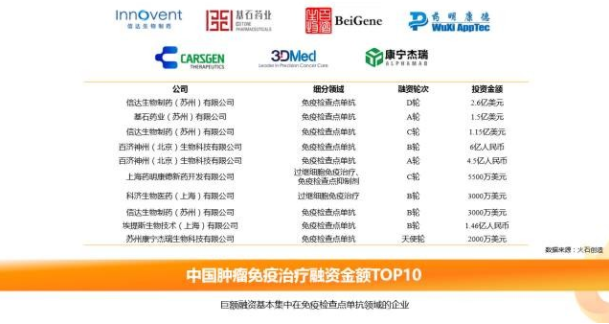
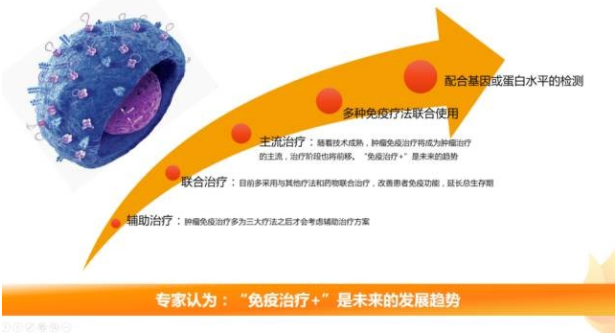
“免疫治疗+”将成为未来趋势
早前,肿瘤免疫治疗大多作为三大疗法之后才考虑的辅助治疗方案,用于维持肿瘤稳定,降低放化疗的副作用。随着研究和临床试验的深入,目前临床上大多将免疫疗法联合药物治疗,改善患者免疫功能,清楚肿瘤微小残留,延长总生存期。越来越多的临床试验结果证明,免疫治疗联合用药与传统药物相比对肿瘤存活率的提高约达一倍之余。
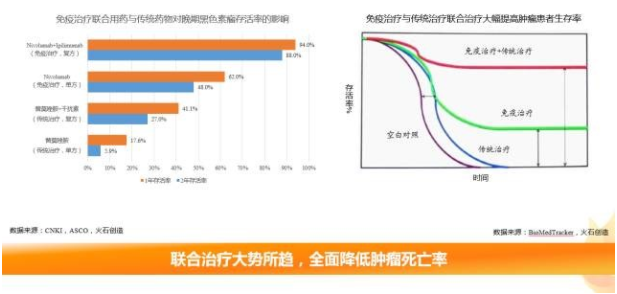
随着研究的进展、技术的成熟,很多专家认为,“免疫治疗+”是未来肿瘤治疗的趋势,目前已经有部分临床试验采取联合使用多种免疫疗法的方案,例如治疗性肿瘤疫苗与免疫检查点单抗联合用药,CAR-T疗法与免疫检查点单抗联合使用等。未来,配合基因或蛋白水平的检测也将深入参与试验,以保证治疗的准确性。